»
Главная
»
ВИЧ и вирус гепатита C: смешанная инфекция
Сочетание ВИЧ-инфекции с гепатитом C встречается часто, что объясняется общими путями передачи
инфекции (парентеральный, половой, вертикальный). В США насчитывается 240 000 таких больных, что
составляет 30% от общего количества ВИЧ-инфицированных.
В некоторых европейских странах частота смешанной инфекции, вызванной ВИЧ и вирусом гепатита C,
еще выше. Так, в Испании гепатит C выявлен по меньшей мере у 50% из 130 000 ВИЧ-инфицированных,
что объясняется широким распространением в/в пути введения наркотиков. Более чем у 90% лиц со
смешанной инфекцией в крови обнаруживают РНК вируса гепатита C (признак хронического гепатита C).
В связи с тем что при заражении через кровь вирус гепатита C по своей контагиозности в 10 раз превосходит ВИЧ, риск смешанной инфекции особенно высок у пациентов, которым переливают кровь и ее
компоненты, а также у потребителей инъекционных наркотиков. При исследовании сывороток, полученных в начале 1990-х гг. (когда еще не был открыт вирус гепатита C) от ВИЧ-инфицированных, больных
гемофилией, более чем в 90% случаев были обнаружены антитела к вирусу гепатита C или его РНК. Вероятность заражения при уколе иглой, загрязненной кровью больного гепатитом C, составляет 2-8%, в то
время как при уколе иглой, инфицированной ВИЧ, вероятность заражения равна лишь 0,3%.
С другой стороны, заражение гепатитом C половым путем происходит значительно реже, чем заражение
гепатитом B и ВИЧ-инфекцией. Этим объясняется сравнительно небольшая частота гепатита C самого по
себе и гепатита C в сочетании с ВИЧ-инфекцией среди гомосексуалистов. Однако в последнее время
появились сообщения об учащении случаев острого гепатита C среди ВИЧ-инфицированных гомосексуалистов, что явно свидетельствует о возможности передачи вируса гепатита C половым путем. Риск
заражения, по-видимому, тем выше, чем больше половых партнеров и чем более вероятно повреждение
слизистых при практикуемой технике секса. В целом примерно 4-8% ВИЧ-инфицированных гомосексуалистов заражены также гепатитом C.
Перинатальная передача вируса гепатита C при нормальном иммунитете происходит редко (менее чем в
1% случаев). Риск инфицирования тем выше, чем более выражен иммунодефицит у ВИЧ-
инфицированной матери, и достигает 20%. С другой стороны, при проведении ВААРТ (наряду с выполнением кесарева сечения) повышения риска передачи вируса гепатита C от ВИЧ-инфицированной матери к ребенку не отмечается.
Течение гепатита C на фоне ВИЧ-инфекции
Течение смешанной инфекции, вызванной ВИЧ и вирусом гепатита C, зависит от тяжести иммунодефицита, обусловленного ВИЧ. Усугубление иммунодефицита ускоряет прогрессирование гепатита C. Впервые это было показано в Американском многоцентровом когортном исследовании гемофилии (MHCS), в
котором у 10% взрослых, страдающих гемофилией, ВИЧ-инфекцией и гепатитом C, после 10-20-летнего
латентного периода развилась печеночная недостаточность, зачастую предшествовавшая появлению
СПИД-индикаторных заболеваний (оппортунистических инфекций и опухолей). Особенно быстрое прогрессирование гепатита C отмечалось у больных с числом лимфоцитов CD4 менее 100 мкл-1. У не инфицированных ВИЧ больных гепатитом C за такой же период наблюдения не было отмечено ни одного
случая печеночной недостаточности. У этих пациентов латентный период, предшествующий развитию
печеночной недостаточности или печеночноклеточного рака, составляет 30-40 лет. Быстрое прогресси-
рование гепатита C на фоне ВИЧ-инфекции было подтверждено в нескольких исследованиях, причем в
некоторых из них использовалась гистологическая верификация диагноза.
Улучшение результатов лечения ВИЧ-инфекции и увеличение продолжительности жизни ВИЧ-
инфицированных повысило вероятность появления у них печеночной недостаточности, вызванной гепатитом C. А снижение летальности от осложнений ВИЧ-инфекции привело к относительному росту летальности от гепатита C. В некоторых лечебных учреждениях печеночная недостаточность стала наиболее частой причиной смерти ВИЧ-инфицированных. Эти данные, наряду с более быстрым прогрессированием гепатита C на фоне ВИЧ-инфекции, побудили многих специалистов рассматривать гепатит C как оппортунистическую инфекцию.
Течение ВИЧ-инфекции на фоне гепатита C
Изучение влияния гепатита C на течение ВИЧ-инфекции вначале дало противоречивые результаты. По
данным когортного исследования, проведенного в Швейцарии, гепатит C является независимым фактором риска быстрого прогрессирования ВИЧ-инфекции до СПИДа и летального исхода. Как оказалось,
это было обусловлено не плохой переносимостью ВААРТ и не редким ее применением, а более слабым
увеличением количества лимфоцитов CD4 под действием антиретровирусных препаратов. Однако по мере увеличения срока наблюдения за больными это различие стиралось. По данным других исследований
(например, когортного исследования Университета Джона Хопкинса и EuroSIDA), гепатит C не оказывает влияния на темпы прогрессирования ВИЧ-инфекции, особенно если при анализе результатов учитывать проведение ВААРТ и ее эффективность. Подытоживая результаты различных исследований, можно
сделать вывод, что гепатит C на течение ВИЧ-инфекции существенно не влияет.
Течение гепатита C на фоне ВААРТ
ВААРТ позволяет добиться более благоприятного течения гепатита C у ВИЧ-инфицированных. Более
того, улучшая функцию иммунной системы, ВААРТ позволяет отсрочить развитие печеночной недостаточности. Этот эффект особенно выражен при лечении ингибиторами протеазы.
С другой стороны, при гепатите С повышается риск гепатотоксического действия некоторых антиретровирусных препаратов. Выраженный гепатотоксический эффект становится причиной прекращения ВААРТ у 10% больных. Этот эффект особенно выражен у невирапина и трех нуклеозидных ингибиторов
обратной транскриптазы: диданозина, зальцитабина и ставудина. Назначать эти препараты больным со
смешанной инфекцией, вызванной ВИЧ и вирусом гепатита C, нежелательно.
У некоторых ВИЧ-инфицированных, страдающих гепатитом C, после начала ВААРТ отмечается временное повышение активности аминотрансфераз в крови. Этот эффект, по-видимому, объясняется усилением воспалительного процесса вследствие улучшения функции иммунной системы. Однако дальнейшее наблюдение за больными свидетельствует о благоприятных сдвигах в течении гепатита C. Назначая
ВААРТ больным со смешанной инфекцией, вызванной ВИЧ и вирусом гепатита C, следует проявлять
особую осторожность.
Диагностика гепатита C на фоне ВИЧ-инфекции проводится так же, как у не инфицированных ВИЧ
больных. Выявление антител к вирусу гепатита C свидетельствует о заражении этой инфекцией, но не
позволяет судить о том, является ли она хронической или у больного наступило излечение. Хронический
гепатит C диагностируют на основании виремии, то есть наличия в крови РНК вируса гепатита C. Следует помнить, что у ВИЧ-инфицированных вследствие угнетения иммунитета антитела к вирусу гепатита C
могут исчезнуть. Поэтому даже в отсутствие этих антител при выраженном иммунодефиците или при
подозрении на хронический гепатит C целесообразно определить уровень РНК вируса гепатита C. Этот
анализ следует выполнить также при подозрении на острый гепатит C, так как антитела у таких больных
появляются лишь спустя 1-5 месяцев после заражения.
У больных со смешанной инфекцией, вызванной ВИЧ и вирусом гепатита C, уровень РНК вируса гепатита C в крови значительно выше, чем у не инфицированных ВИЧ пациентов. С нарастанием виремии
повышается риск перинатального заражения и передачи гепатита C при половых контактах. Однако степень виремии не влияет на течение гепатита C. При концентрации РНК вируса гепатита C в крови менее
2 млн копий в 1 мл вероятность излечения значительно выше, чем при концентрации более 2 млн копий в
1 мл.
Для подбора схемы лечения гепатита C необходимо знать генотип возбудителя. К настоящему времени
известны шесть генотипов вируса гепатита C (каждый со множеством подтипов), которые отличаются по
географии распространения. Так, генотипы 1 и 3 распространены в основном в Европе, в то время как
генотипы 4 и 5 обнаруживаются в Африке, а генотип 6 — в Азии. Генотипирование имеет прогностическое значение. Например, при гепатите C, вызванном генотипами 2 или 3, лечение интерфероном особенно эффективно. У одного и того же больного могут обнаруживаться несколько генотипов вируса гепатита C.
Обязательно определяют активность аминотрансфераз, маркеры холестаза и показатели синтетической
функции печени (активность холинэстеразы, уровни альбумина и общего белка, факторы свертывания
крови). Значения этих показателей трактуются так же, как в отсутствие ВИЧ-инфекции.
Вопрос о целесообразности биопсии печени перед началом лечения гепатита C окончательно не решен и
четких рекомендаций на этот счет, основанных на клиническом опыте, нет. С одной стороны, существует
мнение, что терапию гепатита C можно назначать только при гистологически подтвержденном диагнозе,
учитывая многочисленные побочные эффекты и относительно невысокую эффективность препаратов, а
также их взаимодействия с антиретровирусными средствами. С другой стороны, нельзя забывать, что
проведение такой терапии у больных со смешанной инфекцией почти всегда оправдано ввиду быстрых
темпов прогрессирования гепатита C на фоне ВИЧ-инфекции и развития фиброза или цирроза печени
почти у половины таких пациентов. Следует учитывать и то, что в связи с быстрым прогрессированием
заболевания биопсию печени необходимо выполнять повторно, каждые 2-3 года, а к этому готовы далеко
не все больные. Поэтому в настоящее время биопсия печени считается желательной, но не обязательной
процедурой. Она требуется в тех случаях, когда картина остается неясной и необходимо установить активность гепатита и стадию заболевания, то есть степень поражения паренхимы печени. В основу гистологической классификации гепатита положены градация фиброза (степени F0-F4) и индекс гистологической активности по Кноделю. В отсутствие фиброза и при невысокой активности воспалительного процесса лечение обычно не требуется.
Прежде чем выполнить биопсию печени, следует выяснить, нет ли к ней противопоказаний. Это особен-
но важно для больных гемофилией. При этом заболевании биопсия печени часто бывает противопоказа-
на из-за риска кровотечения.
Если на основании клинической картины возникает подозрение на внепеченочное поражение (васкулит,
гломерулонефрит, криоглобулинемию), могут потребоваться дополнительные исследования, например
биопсия кожи, анализ мочи, биопсия почки, анализ крови на криоглобулины.
Жестких рекомендаций для исследования крови на аутоантитела при подозрении на аутоиммунное заболевание нет. Кроме того, интерпретировать результаты этих исследований нелегко. Примерно у 60%
больных гепатитом C в крови обнаруживают аутоантитела, в частности антинуклеарные, ревматоидный
фактор, антитела к кардиолипину, к гладким мышцам, к микросомальным антигенам печени и почек (анти-LKM1), которые, однако, не имеют какого-либо клинического значения. Если на фоне терапии интерфероном титр этих антител возрастает (или они появляются впервые), необходимости в отмене препарата обычно не возникает. Таким образом, целесообразность анализа крови на аутоантитела сомнительна.
Тем не менее, перед назначением интерферона для исключения аутоиммунного гепатита необходимо определить титр антител к микросомальным антигенам печени и почек (анти-LKM1). В случае положительного результата необходим тщательный контроль за функцией печени во время лечения интерфероном; ухудшение функции печени свидетельствует об активности аутоиммунного гепатита. В этом случае
интерферон отменяют. Вопрос о назначении иммуносупрессивной терапии в каждом случае решается
индивидуально.
Перед тем как назначить интерферон, следует определить уровень ТТГ для исключения поражения щитовидной железы. При нормальной функции щитовидной железы этот анализ проводят каждые
12 недель. Больным, у которых выявлен гипотиреоз, перед назначением интерферона рекомендуется
провести заместительную терапию левотироксином. В случае гипертиреоза назначают антитиреоидные
средства. После коррекции функции щитовидной железы начинают лечение интерфероном, тщательно
контролируя уровень ТТГ в крови (каждые 4 недели). Функция щитовидной железы при терапии интерфероном нарушается примерно у 5% больных, обычно в первые три месяца лечения. При развитии гипотиреоза терапию интерфероном можно продолжить, одновременно назначив левотироксин. При появлении первых признаков гипертиреоза большинство специалистов интерферон отменяют, хотя в некоторых
случаях лечение можно было бы продолжить. После отмены интерферона у большинства больных функция щитовидной железы нормализуется. Но иногда дисфункция сохраняется, и тактика лечения определяется клиническими особенностями каждого случая.
У 12% больных гепатитом C, которым назначают интерферон, перед началом лечения в крови выявляют
антитиреоидные антитела, в частности аутоантитела к йодидпероксидазе, тиреоглобулину и рецептору
ТТГ. У этих больных риск нарушения функции щитовидной железы при лечении интерфероном значительно выше. Если есть возможность, антитиреоидные антитела перед назначением интерферона следует
определять всем больным. Для тех из них, у кого выявлена дисфункция щитовидной железы (по уровню
ТТГ), это исследование является обязательным: с полученным титром будут сравниваться титры антитиреоидных антител, определяемые в процессе лечения.
Цель лечения — добиться полного исчезновения из крови РНК вируса гепатита C. Если РНК вируса гепатита C отсутствует в крови через шесть месяцев после завершения лечения, говорят о достижении
стойкой ремиссии.
Исчезновение РНК вируса гепатита C из крови к моменту завершения лечения называют ремиссией, достигнутой к концу лечения. Если лечение сопровождается нормализацией активности аминотрансфераз в
крови, говорят о биохимической ремиссии. Однако корреляции между биохимической ремиссией и
дальнейшим течением гепатита C нет, поэтому биохимические показатели в качестве критерия эффективности лечения в настоящее время не используются. При сохранении признаков гепатита говорят о неэффективности лечения.
В дальнейшем, говоря об эффективности лечения, мы будем иметь в виду стойкую ремиссию, так как
только в этом случае возможно обратное развитие фиброза и внепеченочных поражений и только в этом
случае исключается дальнейшая передача инфекции.
Повторное появление в крови РНК вируса гепатита C, которую в течение какого-то времени после лечения не удавалось выявить, свидетельствует о рецидиве гепатита C. Вероятность рецидива особенно высока в течение первого месяца после завершения терапии, затем она постепенно уменьшается. Поэтому о
результатах лечения судят по прошествии шести месяцев. У отдельных больных рецидив может наступить и в более поздние сроки, иногда даже через несколько лет. Поэтому даже после успешного лечения
необходимо длительное наблюдение, включающее определение активности аминотрансфераз в крови, а
при подозрении на рецидив — РНК вируса гепатита C.
Для лечения гепатита C используют интерфероны и аналоги нуклеозидов. Интерфероны представляют
собой гликопротеиды, которые защищают клетки, ингибируя трансляцию вирусной мРНК и препятствуя
проникновению вирусов в клетки, а также выделению их в кровь. Кроме того, интерфероны благоприятно влияют на иммунитет, оказывая модулирующее действие на цитокины. Из аналогов нуклеозидов применяется производное гуанозина рибавирин. Больным, у которых развился цирроз печени и лечение интерфероном неэффективно, можно предложить трансплантацию печени.
Лечение гепатита C у ВИЧ-инфицированных имеет две особенности. Во-первых, стойкие ремиссии наблюдаются реже из-за выраженного иммунодефицита, во-вторых, лечение чаще приходится прекращать
из-за развития побочных эффектов.
Интерферон ? в виде монотерапии и в сочетании с рибавирином утратил свое значение, так как эффективен лишь у 13-40% больных, а в 30% случаев его приходится отменять из-за побочных эффектов. Поэтому вместо обычного интерферона (например, интерферона ?-2a и интерферона ?-2b) стали применять
пегилированный интерферон, то есть связанный с полиэтиленгликолем (PEG). Полиэтиленгликоль, защищая молекулу интерферона от расщепления ферментами, значительно удлиняет его период полувыведения. Кроме того, благодаря более медленному всасыванию снижается максимальная сывороточная
концентрация препарата, что способствует уменьшению побочных эффектов, и в то же время повышаются минимальная и средняя сывороточные концентрации, что увеличивает эффективность лечения. Эти
особенности пегилированного интерферона позволяют назначать его один раз в неделю вместо трех при
лечении обычным интерфероном.
При смешанной инфекции, вызванной ВИЧ и вирусом гепатита C, терапия пегилированным интерфероном в сочетании с рибавирином считается стандартной. Лучшие результаты при такой терапии были получены в исследовании APRICOT (Международное испытание препаратов Пегасис® и рибавирин у коинфицированных больных СПИДом). Это наиболее крупное из проводившихся до настоящего времени
исследований среди ВИЧ-инфицированных, больных гепатитом C (Torriani, 2004). Стойкая ремиссия после 48 недель лечения была достигнута у 40% больных. Лишь у 12% больных терапию пришлось прекратить из-за развития побочных эффектов. Особенно улучшились результаты лечения (по сравнению с терапией обычным интерфероном и рибавирином) у инфицированных генотипом 1 (29%): этот вариант гепатита C характеризуется наименее благоприятным прогнозом. Среди инфицированных генотипами 2
или 3 (варианты гепатита C с более благоприятным прогнозом) стойкой ремиссии достигли 62% больных. Общая частота ремиссий и частота ремиссий среди инфицированных генотипом 1 и генотипами 2
или 3 оказались выше, чем при терапии по схемам «интерферон 2? + рибавирин» (12, 7 и 20% соответственно) и «пегилированный интерферон + плацебо» (20, 14 и 36% соответственно). Продолжительность
лечения всех больных составляла 48 недель независимо от генотипа вируса гепатита C. Примечательно,
что в случае генотипов 2 и 3 частота рецидивов через 72 недели была лишь 2%, в то время как при терапии в течение 24 недель рецидивы отмечались почти в 50% случаев. Следовательно, при гепатите C, вызванном генотипами 2 или 3, длительность лечения тоже должна составлять 48 недель.
Другие исследования, например RIBAVIC и ACTG A5071, не подтвердили результатов, полученных в
исследовании APRICOT. По данным этих двух исследований, стойкой ремиссии при лечении пегилированным интерфероном в сочетании с рибавирином достигли лишь 27% больных. Однако непосредственно сравнивать результаты всех трех исследований трудно из-за методологических различий в их проведении. Например, в исследовании RIBAVIC было больше больных с циррозом печени. Этим,
по-видимому, в какой-то степени объясняется более низкая эффективность лечения. Тем не менее, оба
исследования подтвердили преимущество лечения пегилированным интерфероном в сочетании с рибавирином.
Подробные сведения о рибавирине, обычном и пегилированном интерфероне приводятся в главе, посвященной лекарственным средствам.
Опасение, что назначение интерферона может отрицательно сказаться на течении ВИЧ-инфекции, не
подтвердилось ни в одном из исследований. Напротив, благодаря своему противовирусному действию
интерферон способствовал уменьшению концентрации РНК ВИЧ в крови у большинства больных. Абсолютное количество лимфоцитов CD4 может несколько уменьшиться вследствие временной лейкопении,
но в процентном отношении их количество обычно возрастает. Ни в одном исследовании, посвященном
интерферону, существенного отрицательного влияния этого препарата на течение ВИЧ-инфекции отмечено не было (Soriano, 2002).
Для больных с резистентным к интерферону гепатитом C и для больных с рецидивами эффективной терапии пока нет. Тем, кто раньше получал монотерапию интерфероном, можно назначить пегилированный интерферон в сочетании с рибавирином. Каких-либо рекомендаций на случай неэффективности пегилированного интерферона нет. Возможно, в будущем найдет применение также консенсусный интерферон.
Лечение острого гепатита C тоже является нерешенной проблемой. У не инфицированных ВИЧ пациентов оказалось очень эффективным лечение интерфероном ?-2b, начатое в течение первых шести месяцев.
Излечение наступило у 98% (!) больных (Jaeckel, 2001). При ретроспективном анализе результатов лечения острого гепатита C у ВИЧ-инфицированных эффект был отмечен у 80% больных. Эти данные подчеркивают важность раннего лечения и при смешанной инфекции, вызванной ВИЧ и вирусом гепатита
C. Проводить лечение таким пациентам желательно в рамках проспективных клинических исследований.
Ниже приводятся рекомендации по лечению гепатита C на фоне ВИЧ-инфекции.
Показания и противопоказания
Поскольку на фоне ВИЧ-инфекции гепатит C прогрессирует более быстрыми темпами и поскольку на
фоне гепатита C возрастает риск гепатотоксического действия антиретровирусных препаратов, у каждого больного со смешанной инфекцией нужно определить показания к лечению. При этом можно руководствоваться алгоритмом, приведенным на рис. 1.
Лечение гепатита C показано при гистологически подтвержденном фиброзе печени со степенью F2-F4.
Внепеченочные проявления гепатита C (васкулит, гломерулонефрит, криоглобулинемия) также являются
показанием к терапии. Следующие прогностические факторы свидетельствуют в пользу эффективности
терапии:
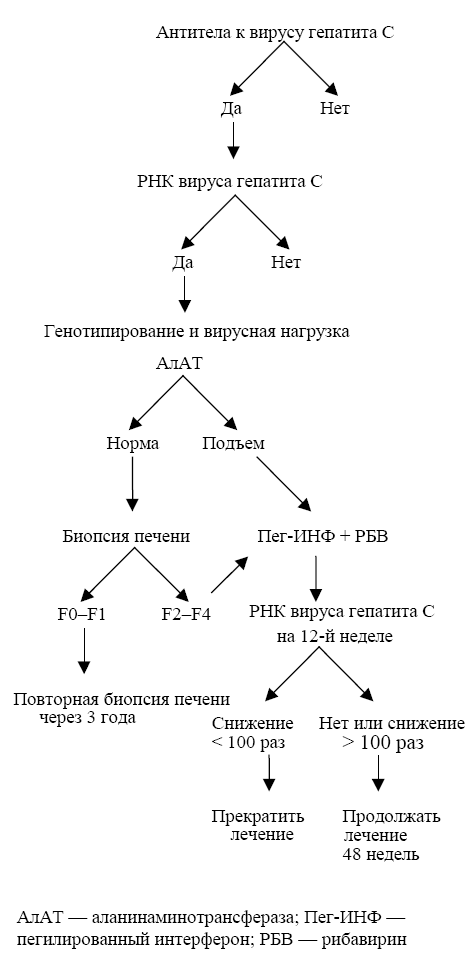
Рисунок 1. Алгоритм лечения гепатита C (приводится с изменениями по Soriano, 2002 и Soriano, 2004)
Следует также учитывать противопоказания к лечению гепатита C, к которым относятся:
Заместительная терапия метадоном или поламидоном не является противопоказанием к лечению гепатита C, если осуществляется тщательный контроль за состоянием больного. Тем не менее, прежде чем
начинать противовирусную терапию у больных наркоманией и алкоголизмом, следует подключить их к
работе специализированных терапевтических программ.
Кроме того, следует учесть состояние иммунной системы больного и проводимую ему противовирусную
терапию (см. ниже).
Если позволяет состояние больного, сначала проводят лечение гепатита C и лишь затем назначают ВААРТ. Такой подход диктуется тем, что на фоне гепатита сильнее проявляется гепатотоксический эффект
антиретровирусных препаратов. Кроме того, гепатит C препятствует нормализации функции иммунной
системы. И наконец, при последовательном лечении устраняется риск лекарственных взаимодействий и
улучшается соблюдение больными врачебных предписаний. Рекомендуется следующая тактика:
| Больные, не получающие ВААРТ |
|
Если количество лимфоцитов CD4 больше 350 мкл-1, можно начать лечение гепатита C. Вопрос о том, следует ли
начинать ВААРТ в случае высокой вирусной нагрузки (более 50 000 копий РНК ВИЧ в 1 мл), остается неясным.
|
| Больные, получающие ВААРТ |
|
Если количество лимфоцитов CD4 на фоне ВААРТ превышает 350 мкл-1, а РНК ВИЧ не определяется, можно начать лечение гепатита C.
|
За несколько недель до начала лечения гепатита C желательно внести необходимые коррективы в антиретровирусную терапию. Лечение можно назначать лишь при стабильном состоянии больного, то есть
при условии подавления репродукции ВИЧ и устранения побочных эффектов ВААРТ.
На фоне терапии гепатита C противопоказан диданозин: он может стать причиной панкреатита, оказывает токсическое действие на митохондрии и способствует декомпенсации цирроза печени. Желательно
также избегать зидовудина, поскольку он приводит к развитию анемии и лейкопении. Опасность побочных эффектов, по-видимому, возрастает и при назначении интерферона одновременно со ставудином
(токсическое действие на митохондрии). Модифицировать антиретровирусную терапию следует так,
чтобы ее эффективность не снизилась. Если обеспечить это невозможно, следует пересмотреть решение
о начале лечения гепатита C.
Стандартное лечение — пегилированный интерферон в сочетании с рибавирином в течение 48 недель
(Soriano, 2004), независимо от генотипа вируса гепатита C (Rockstroh, 2004).
В настоящее время имеются два препарата пегилированного интерферона: Пег-интрон® и Пегасис®.
Пег-интрон® вводят подкожно из расчета 1,5 мкг на 1 кг веса. Пегасис® вводят подкожно в дозе 180 мкг.
Оба препарата назначают 1 раз в неделю. Хранить их следует в холодном месте.
Рибавирин назначают с учетом веса больного в дозе не менее 10,5 мг/кг в сутки. Препарат выпускается в
капсулах. Суточную дозу можно принять сразу или в несколько приемов.
Перед тем как начать лечение, больному следует подробно рассказать о возможных побочных эффектах
препаратов. Обсуждению подлежат три важных аспекта.
Почти у всех больных в начале лечения наблюдается гриппоподобный синдром или недомогание. Поскольку предсказать тяжесть этих симптомов невозможно, прием препаратов желательно начать тогда,
когда на ближайшие дни не планируются важные встречи или другие события, связанные с личной жизнью или профессиональной деятельностью. Удобно, например, начинать прием препаратов накануне выходных. В течение первых дней лечащий врач должен быть доступен для больного. Дополнительно можно назначить парацетамол. Обычно в течение первых 2-4 недель симптомы ослабевают. Поэтому вопрос
об отмене препаратов из-за побочных эффектов следует рассматривать лишь в конце первого месяца лечения.
Большинство больных переносят препараты хорошо и продолжают вести привычный образ жизни. Но
бывает и так, что на несколько дней утрачивается трудоспособность, особенно на первых порах. В редких случаях побочные эффекты бывают настолько выражены, что пациенты теряют трудоспособность на
весь период лечения. Об этом тоже следует заранее предупредить больного.
Пациенты должны знать о тератогенном действии интерферона и рибавирина. Поэтому и во время лечения, и как минимум в течение 6 месяцев после его завершения следует применять надежные средства
контрацепции.
В процессе лечения необходим регулярный контроль за состоянием больных. Вначале обследование
проводят каждые 2 недели, в дальнейшем — не реже одного раза в 4 недели. Лабораторные исследования
включают:
Наиболее важным показателем, позволяющим судить об эффективности лечения гепатита C, является
концентрация РНК вируса гепатита C в крови. Ее нужно определить через 12 недель после начала лечения, чтобы решить вопрос о целесообразности продолжения терапии. Однако на практике этот анализ
часто проводят через 4-8 недель, поскольку демонстрация результатов лечения усиливает мотивацию
больного.
При каждом посещении врача оценивают психический статус больного, учитывая при этом информацию,
полученную от членов семьи больного и его близких.
Устранение побочных эффектов имеет решающее значение для успеха лечения. Большое количество
случаев прекращения лечения в прошлом, по-видимому, объясняется отсутствием опыта комбинированной терапии. Устранение побочных эффектов, по-видимому, существенно повышает частоту стойких
ремиссий. Больному нужно объяснить, что побочные эффекты пройдут после завершения лечения.
Рибавирин у 20% больных вызывает гемолитическую анемию. Это осложнение лечат эпоэтином y. Дозы
препарата, рекомендуемые разными специалистами, различаются. Обычно назначают примерно 100
МЕ/кг подкожно 3 раза в неделю. При необходимости дозу рибавирина можно уменьшить вдвое (при
уровне гемоглобина ниже 10 г%) или совсем отменить этот препарат (при уровне гемоглобина ниже 8,5
г%). Однако к уменьшению дозы рибавирина и его отмене, часто практиковавшимся в прошлом, сейчас
прибегают только в том случае, если не помогает эпоэтин. Недавние исследования показали важную
роль подбора оптимальной дозы рибавирина в успехе лечения. Для снижения токсического действия на
костный мозг рекомендуется назначать фолиевую кислоту в дозе 5 мг/сут.
Препараты гранулоцитарного колониестимулирующего фактора (Г-КСФ) ослабляют лейкопению, вызываемую интерфероном. Клинический опыт по применению этих препаратов пока небольшой. Однако,
учитывая нежелательность снижения дозы интерферона при развитии лейкопении, назначение препаратов Г-КСФ представляется целесообразным.
Для лечения легкой депрессии, вызываемой интерфероном, рекомендуется пароксетин (20 мг/сут), который обычно хорошо переносится. При глубокой депрессии или появлении у больного суицидальных
мыслей интерферон следует отменить.
Часто наблюдаемое похудание требует диетотерапии. Очень важно, особенно при стационарном лечении
страдающих наркоманией, чтобы пища соответствовала вкусовым пристрастиям пациентов. Возможно,
похудание является следствием липоатрофии, поэтому по возможности следует использовать те аналоги
нуклеозидов, у которых липодистрофическое действие минимально.
При лечении интерфероном возможно нарушение функции щитовидной железы (см. выше), которое может потребовать отмены препарата.
Продолжительность лечения зависит от его эффективности. Если спустя 12 недель в крови еще выявляется РНК вируса гепатита C, лечение прекращают независимо от генотипа возбудителя. Вероятность ремиссии у таких больных низка. Раньше рекомендовали продолжать лечение до истечения 24 недель, объясняя это более медленной элиминацией вируса гепатита C на фоне ВИЧ-инфекции. Однако в настоящее
время даже у ВИЧ-инфицированных решение о прекращении лечения гепатита C можно принять через
12 недель.
Если концентрация РНК вируса гепатита C к этому времени снизилась на два порядка и более или РНК
вируса гепатита C не определяется, лечение продолжают еще в течение 36 недель при всех генотипах вируса. Раньше в случае генотипов 2 и 3 рекомендовали завершать лечение после 24 недель. Однако последние данные, полученные в исследовании APRICOT, свидетельствуют об очень низкой частоте рецидивов (2%), когда лечение длится 48 недель, в то время как в более ранних исследованиях, где продолжительность лечения составляла 24 недели, рецидивы наблюдались у 50% больных. Поэтому у всех
больных независимо от генотипа вируса гепатита C лечение должно длиться 48 недель. Продолжение лечения сверх этого срока у больных с генотипами 1 и 4, по-видимому, способно привести к дальнейшему
уменьшению частоты рецидивов.
Рекомендации по лечению гепатита C постоянно обновляются. Поэтому при необходимости получения
каких-либо разъяснений следует связываться с ведущими клиниками, занимающимися данной проблемой.
Смешанную инфекцию, вызванную ВИЧ и вирусом гепатита C, лечить нелегко. Поэтому при любой возможности таких больных нужно включать в клинические исследования.
Источник: www.eurasiahealth.org